只需通过简单的一滴血就能成功的检测肿瘤,并且针对肿瘤患者快速确定一项治疗方案是否适合,还可以继续监测该治疗方案在癌细胞产生耐药之后的效果。这就是曾经荣登2015年度MITTechnology Review十大突破技术榜单的“液体活检”技术!而循环肿瘤DNA(circulatingtumor DNA, ctDNA)检测便是“液体活检”技术之一。
那到底什么是ctDNA?有什么用?能干什么?适用于哪些人?本文将以头颈肿瘤为例,详细介绍ctDNA在临床肿瘤的诊断、用药指导、肿瘤进展检测及预后等方面的应用。
一、ctDNA背景
1、ctDNA临床意义及应用范围
肿瘤细胞破裂后,细胞中的DNA释放到血液中,这些DNA被称为循环肿瘤DNA(ctDNA),与胎儿DNA可进入母体外周血类似。这些DNA片段携带有相对完整的癌细胞基因组变异信息,包括SNP(点突变)、InDel(插入缺失)、CNV(拷贝数变异)、fusion(融合基因)等。因此,ctDNA可以全面反映癌组织的DNA变异情况。
表一.ctDNA研究进展
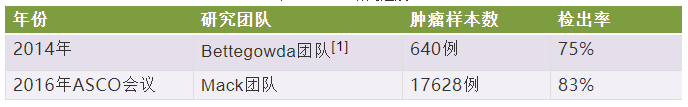
检出肿瘤类型:结直肠癌、胰腺癌、膀胱癌、乳腺癌、胰腺癌、胃癌、卵巢癌、黑色素瘤、头颈癌和肝癌等
Dawson等[2]研究发现,ctDNA检测作为一种无创的检测方法,能够真实的反映实体肿瘤组织中的基因突变图谱和频率,是治疗效果的评估及治疗后临床随访的重要检测指标,尤其在一些有典型临床症状、检查却无特异性以及诊断困难的肿瘤中,可以避免复杂的、有创伤性的活检,也能避免穿刺活检所导致的肿瘤转移风险。
2、目前ctDNA的主要检测手段和缺陷
ctDNA检测突变的最大难题是:众多超低频突变。含有突变的ctDNA仅占cfDNA的0.01-1%,在晚期癌症中也仅能达到10%左右的量级,因此如何在大量正常DNA中分辨出超低频突变就成为了一大难题。
表二.各大类技术的检测突变下限
之所以难以继续下探主要是由于PCR体系中的“马太效应”,即含有低频突变的片段在几十个PCR扩增循环中会被占绝对主导地位的正常版本片段所掩盖掉。针对ctDNA超低频突变特点,目前只有数字PCR(DigitalPCR, dPCR)和暴力测序法可能达到更低的检测下限。
dPCR的原理是将溶液模板分成大量小液滴,分配到不同的反应单元,再分别进行PCR扩增,检测阳性液滴数量,根据泊松分布进行绝对定量(图一)。这种方法的优点是可以避免低频突变信号被淹没在大量正常信号中,缺点是通量低,一次只能检测一个位点,而且仪器价格昂贵。
随后发展的BEAMing技术,是一种增强型dPCR。原理是在磁珠上进行dPCR后,利用荧光探针来区分基因是否发生突变,再用流式细胞仪分析荧光分布(图二)。这种增强型dPCR方法使得PCR定量更准确,也可以实现同时检测少量几个位点,而缺点是价格比普通的dPCR还贵,且还需要流式细胞仪。
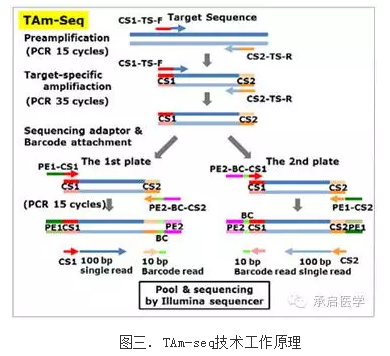
TAm-seq技术,即标记扩增深度测序,是使用标记扩增之后进行高达10000×以上的超深度测序(图三)。这种方法理论上可以检测出非特定的极低频突变,但是成本非常高。加上此方法是进行两次PCR扩增,增大了其偏好性(图一左边的情形),并且不可避免的出现测序仪器误差,对算法要求极高,因此实际的稳定检出下限只有1-2%左右。
此外,癌症个体化深度测序(CAPP-seq)技术[3]为了解决多位点、高偏好性下测序成本高的问题,则采取尽量减少检测位点数量策略。此策略首先对肿瘤组织的外显子组或者全基因组进行测序,获得个体特有的肿瘤突变,再根据此分析结果设计少量的检测位点进行ctDNA深度测序。且不说此技术的优点,单从“液体活检”、“无创活检”理念出发,CAPP-seq技术就不符合要求,因为CAPP-seq技术首先要求对肿瘤组织进行测序,这就使得个体定制化商业成本非常高。
另外,ctDNA的保存和提取也是ctDNA检测突变所面临的另一个挑战。首先采血的保存和运输遇到的冷冻问题导致提取量极不稳定;而保存运输以及血浆的制备过程中出现的微量溶血也会造成提取ctDNA失败,即使使用昂贵的专用ctDNA采血管,实测溶血率也很高。
二、技术发展更新
针对目前国内外对ctDNA的检测手段存在的困难,有相关企业经过不断钻研、创新,给出了一个强有力的解决方案,结合ddPCR(DropletDigital PCR)系统的低偏好性和大规模测序的多重位点检测能力和未知突变的检测能力,自主研发的低成本ctDNA提取和保存方法,以及高精度全自动化的云平台,使得ctDNA的检测难题迎刃而解。
1、低偏好性RaindanceddPCR系统扩增
采用RaindanceddPCR系统。ddPCR系统的灵敏度主要由液滴数量和液滴体积两个参数共同决定,液滴数量越多、液滴体积越小,系统的性能就越高。与传统的Bio-rad系统20000个液滴相比Raindance拥有800倍的液滴数量(总共1600万液滴),可以检测更高的动态范围以及更低的检测下限。而相比于Bio-rad850pL的液滴体积,Raindancedd PCR液滴体积要小得多(4.4pL),可以提高局部模板浓度,提高扩增效率,同时检测更多的位点(图四)。此外,Raindance目前还推出2款配套试剂盒,在样本起始量低至10ngDNA的情况下,即可使97%的序列覆盖度达到500×,实现对FFPE、组织样品中50个肿瘤基因序列(230对扩增引物)和血液中49个肿瘤基因序列(548对扩增引物)进行靶向富集和分析,内容全面,覆盖度高,例如AML、MDS、MPN等,还包括比较难检测的CEBPA和NOTCH1基因等。
此外,Raindance ddPCR系统的试剂兼容性较好,可与Raindance仪器生产厂家建立合作关系,取得其技术支持,在定制开发方面打造优势。
2、测序和分析策略
采用Illumina/ion平台,根据不同的测序目的进行测序策略调整以及测序平台的选择:偏重科研性质、对成本较为敏感的可选择Illumina平台;偏重临床应用,对速度较为敏感的可选择iontorrent平台。根据目标需求,可实现单位点或多位点同时测序,且可覆盖临近区段,检测未知突变。
依托高精度FANSe系列算法,可保证测序数据分析的可靠性,利用基因云分析平台实现快速自动化分析,操作简便,价格更实惠。
3、低成本cfDNA稳定保存和提取
采用创新的促凝管方法提取cfDNA,可低成本的稳定保存和提取cfDNA。试验低成本cfDNA稳定保存和提取方案,若以怀孕<8周孕妇外周血为例,胎儿DNA在母体cfDNA中的比例在0.5%以下情况下,利用自主研发的促凝管方法检测男婴的Y染色体基因座(多重PCR)。结果发现,该低成本方案,cfDNA冷藏2周后提取无降解,较难扩增的第2、3管效果甚至明显好于传统当场立即提取方案。
参考文献
[1]Bettegowda C, Sausen M, Leary RJ, Kinde I, Wang Y, Agrawal N, et al. Detectionof circulating tumor DNA in early- and late-stage human malignancies. Sciencetranslational medicine. 2014;6:224ra24.
[2] Dawson SJ,Tsui DW, Murtaza M, Biggs H, Rueda OM, Chin SF, et al. Analysis of circulatingtumor DNA to monitor metastatic breast cancer. The New England journal ofmedicine. 2013;368:1199-209.
[3] Newman AM,Bratman SV, To J, Wynne JF, Eclov NC, Modlin LA, et al. An ultrasensitivemethod for quantitating circulating tumor DNA with broad patient coverage.Nature medicine. 2014;20:548-54.
本文地址:https://www.guokang.com/yixuexindongtai/33.html

 深圳
深圳